Ученые раскрыли уникальный биофизический механизм, позволяющий возбудителям туберкулеза выживать внутри человеческих клеток. Эта находка открывает перспективы для создания новых стратегий борьбы с одной из самых опасных инфекций на планете.
Туберкулез продолжает оставаться глобальной проблемой, унося жизни более миллиона человек ежегодно, особенно в странах Азии, Африки и Латинской Америки. Эволюция наделила микобактерии сложными инструментами для захвата иммунных клеток и уклонения от уничтожения.
«В Индии туберкулез остается серьезной угрозой, — рассказывает Аюш Панда. — Я вырос в регионе, где вспышки заболевания часты, и всегда стремился понять механизмы распространения инфекций. Именно это стало моим научным призванием».
Хитроумный механизм выживания
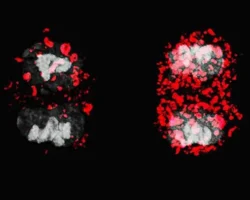
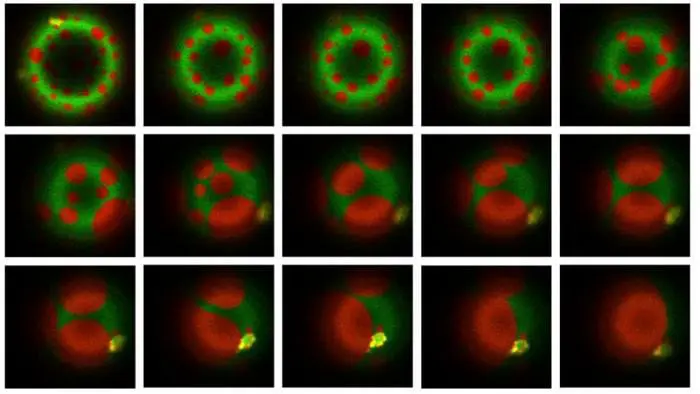
Исследование показало, что микобактерии выделяют крошечные внеклеточные везикулы. Эти частицы сливаются с оболочками иммунных клеток, доставляя особые липиды (жировые молекулы), которые значительно повышают жесткость клеточной мембраны.
Сбой в работе иммунной защиты
В норме иммунные клетки поглощают бактерии, заключая их в фагосому, которая затем сливается с лизосомой – «переварочным цехом» клетки, заполненным разрушительными ферментами. Ученые выяснили, что микобактерии блокируют это слияние, искусственно уплотняя мембрану фагосомы, создавая вокруг себя защитный барьер.
«Жесткая мембрана мешает фагосоме соединиться с лизосомой, — поясняет Панда. — Это изящный биофизический трюк: бактерии меняют структуру мембраны, чтобы избежать гибели». Удивительно, но везикулы могут влиять даже на соседние, еще не инфицированные иммунные клетки, ослабляя их заранее.
Новый взгляд: роль липидов
Открытие предлагает революционный подход к пониманию выживаемости микобактерий. Если ранее наука фокусировалась на разрушающих бактерии белках, то эта работа демонстрирует ключевую роль липидов. Сам факт внедрения бактериальных липидов в мембраны хозяина достаточен для нарушения иммунной функции.
«Поразительно, но введение микобактериальных липидов в искусственные мембраны, имитирующие фагосомы, полностью меняло их физические свойства», — подчеркивает Панда.
Перспективы для новых методов лечения
Ученые зафиксировали схожие мембранные эффекты, вызванные везикулами других патогенов – Klebsiella pneumoniae и Staphylococcus aureus. Это указывает на универсальную эволюционную стратегию. Результаты исследования открывают несколько оптимистичных путей для разработки терапии: воздействие на белки, формирующие бактериальные везикулы, или нейтрализацию эффекта уплотнения мембран.
«Теперь, зная механизм защиты бактерий, мы можем искать способы его преодолеть, — уверен Панда. — Если помешать бактериям уплотнять мембраны, иммунная система получит шанс полностью обезвредить угрозу».
Источник: scientificrussia.ru