Ученые Института цитологии РАН (ИНЦ РАН) впервые установили структуру и геометрические параметры «коротких олигомеров» актина. Эта форма белка накапливается в клетках при стрессе и нейродегенеративных патологиях, включая болезни Хантингтона и Альцгеймера. Полученные результаты крайне важны для понимания причин дегенеративных нарушений нервной системы. Они открывают перспективы для разработки методов ранней диагностики этих тяжелых заболеваний.
Актин и его ключевые формы в клетке
Актин — один из самых распространенных белков в клетках эукариот (растений, грибов, животных, человека). Известны две основные формы: мономерный G-актин и полимерный F-актин, представляющий собой цепочку из G-мономеров. F-актин критически важен для работы мышц и цитоскелета. G-актин, находясь в цитоплазме, также участвует в ключевых ядерных процессах, включая функционирование ДНК.
Третье состояние: инактивированный актин (I-актин)
Помимо G- и F-форм, существует состояние актина, первоначально считавшееся промежуточным и названное «инактивированным актином» (I-актин). Однако исследования ИНЦ РАН доказали, что I-актин — это особая структура из 14-16 мономеров, чья архитектура отличается от G-актина.
Роль I-актина в нейродегенеративных заболеваниях
Интерес к структуре I-актина связан с его накоплением в виде «коротких олигомеров» при стрессе и нейродегенеративных болезнях. Эти олигомеры отличаются от полимерного F-актина и являются потенциальной мишенью для терапии Альцгеймера и Хантингтона. До сих пор механизмы их образования и точная структура оставались неизвестными.
Модель образования и параметры олигомеров
Ученые выдвинули гипотезу, что основой «коротких олигомеров» ядерного актина служит I-актин. В ходе работы была впервые предложена многоступенчатая модель их образования и установлены ключевые параметры: размер, форма и принцип сборки.
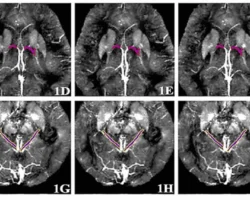
Данные метода SEC-SAXS (определяющего форму, размер и агрегатное состояние биомолекул в растворе) и электронной микроскопии подтвердили, что «короткие олигомеры» — это I-актин. Он имеет форму плоских дискообразных «бусинок» радиусом примерно 8-9 нанометров.
Характеристика структуры «бусинок»
Структура «бусинок» I-актина исследована методами собственной триптофановой флуоресценции, флуоресценции гидрофобного зонда АНС и время-разрешенной анизотропии флуоресценции. Установлено, что «бусинки» способны собираться в вытянутые цепочки, напоминающие структуру F-актина («бусинки на ниточке»), но значительно толще и короче.
Значение открытия для медицины
Определение структуры «коротких олигомеров» актина, их субъединиц и факторов сборки — важнейший шаг к пониманию причин развития нейродегенеративных заболеваний. Это открывает широкие возможности как для их раннего выявления, так и для разработки эффективных терапевтических стратегий.
Работа выполнена совместно с учеными Научно-исследовательского центра молекулярных механизмов старения и возрастных заболеваний Московского физико-технического института (МФТИ) при поддержке гранта РНФ 23-15-00494.
Информация предоставлена пресс-службой Института цитологии Российской академии наук.
Источник фото: ru.123rf.com
Источник: scientificrussia.ru